我院高峰课题组近日在化学类顶级期刊Angewandte Chemie International Edition上在线发表研究论文,报道了一个全新骨架倍半萜的分离鉴定、仿生全合成及神经保护活性。
活性新骨架天然产物的发现与合成是天然药物化学研究的重点领域,也是人类新药研发的重要源泉。紫茎泽兰(Eupatorium adenophorumSpreng)是菊科泽兰属植物,是我国头号外来入侵物种,对生态环境及农林牧业产生了严重危害。
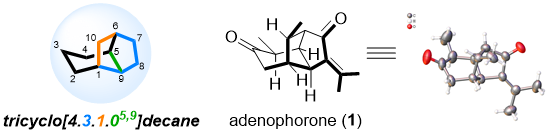
图1. Adenophorone结构
高峰教授课题组从紫茎泽兰植物的叶子中首次发现一个具有独特笼状三环[4.1.05,9]癸烷结构的倍半萜类新骨架化合物—(−)-adenophorone(1)(图1),通过NMR及X-Ray鉴定了该新骨架倍半萜的结构,并基于仿生策略高效简洁地完成了新化合物的不对称全合成研究。
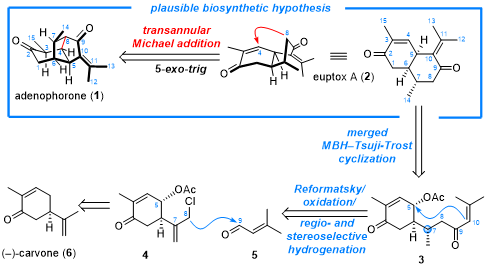
图2.Adenophorone的逆合成策略分析
在生源途径推测过程中,作者分析天然产物(+)-euptox A(2)可能是(−)-adenophorone的重要生物合成前体,转化的关键则在于(+)-euptox A的C4位和C8位环合后可形成(−)-adenophorone核心骨架结构。故受生源合成推测的启发,在仿生逆合成思路中(图2),作者希望通过从商业可得的(−)-carvone(6)出发,通过Reformatsky/氧化/区域和立体选择性氢化、MBH-Tsuji-Trost环化等反应实现生源前体(+)-euptox A的合成,在此基础上再经跨环Michael加成高效简洁地完成(−)-adenophorone的仿生构建。
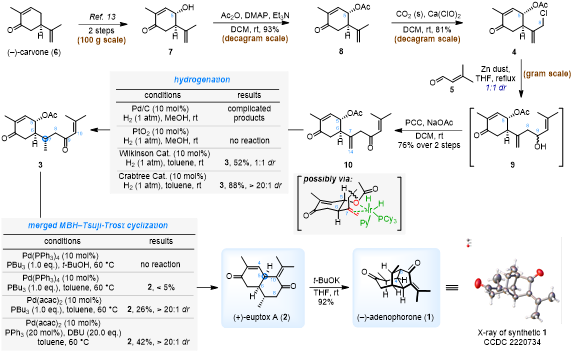
图3. Adenophorone的不对称全合成路线
首先,作者利用市售的6为原料,通过Mukaiyama不对称氧化反应合成具5α-OH的产物7;7在碱性条件与Ac2O反应获得乙酰化产物8,进而与Ca(ClO)2反应,在C8位成功引入Cl,获得产物4;在THF回流,Zn粉还原的条件下,通过Reformatsky反应合成中间体9(dr 1:1)。值得一提的是,在此过程中化合物9可以由廉价易得的原料6经4步反应,以克级规模实现高效制备。随后,非对映异构体9未经纯化,经氯铬酸吡啶鎓盐(PCC)、NaOAc氧化生成α,β-不饱和酮10。化合物10中C(7)-C(10)双键的区域及立体选择性氢化可在Crabtree催化条件下实现,以dr值>20:1、88%的高收率获得化合物3,实现手性中心C7位的构建。接下来,作者考虑利用MBH-Tsuji-Trost环化构建C(5)-C(10)键,期望生成顺式稠和的双环结构2。经反应条件筛,确定了以Pd(acac)2为催化剂、PPh3为配体、DBU为碱、甲苯为溶剂的最佳反应条件,以42%收率实现了双环单元的构建。最后,经过分子内Michael加成反应顺利地得到了预期的笼状三环核心骨架产物1(图3)。合成化合物1的结构及绝对构型通过X单晶衍射分析加以确定。至此,基于仿生合成策略,完成了(−)-adenophorone的首例不对称全合成,并验证了由2到1的生物合成假设。此外,(−)-adenophorone对H2O2处理的SH-SY5Y和PC12细胞损伤模型表现出优越的神经保护活性,为天然源神经保护剂先导化合物的开发提供新的参考。
该项工作涵盖天然产物化学研究的全过程,包括提取分离、结构鉴定、生源推测、半合成,仿生全合成及生物活性研究。从大量易得的(−)-carvone出发,首次完成具神经保护活性天然产物(−)-adenophorone的全合成,对于利用新骨架天然产物开发活性先导化合物具有积极意义。
上述成果近期在Angewandte Chemie International Edition发表,第一作者是西南交通大学博士研究生尹博,通讯作者为四川大学华西药学院唐培教授和西南交通大学高峰教授。
论文信息:

